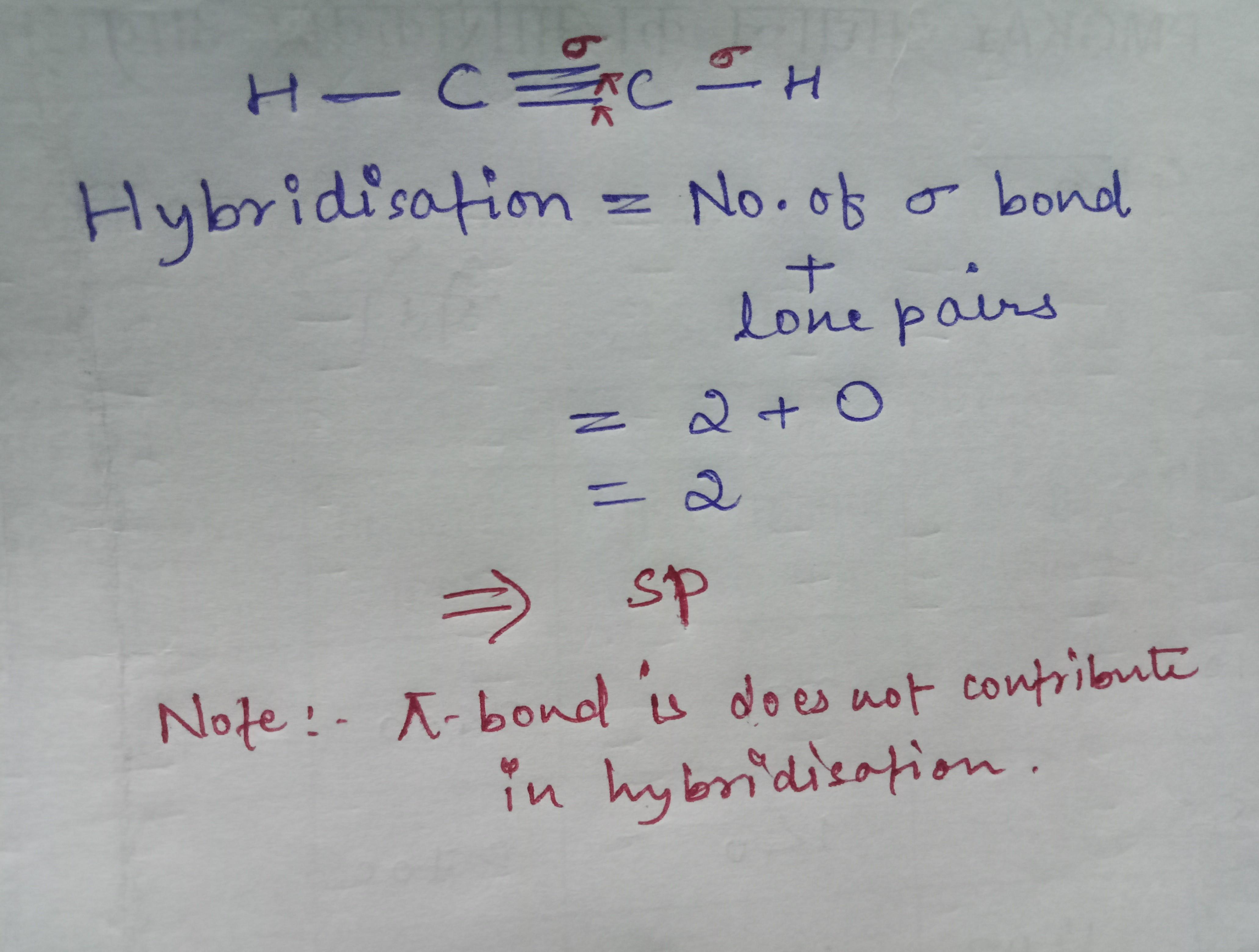C2H2 مالیکیول، جسے ایتھائین یا ایٹھیلین بھی کہا جاتا ہے، کی کیمیائی ساخت میں اہم خصوصیات موجود ہیں۔ اس مالیکیول میں کاربن اور ہائیڈروجن کے ایٹمز کا تعلق ایک خاص طریقے سے قائم ہوتا ہے، جس کے نتیجے میں کئی covalent bonds بنتے ہیں۔
اس کے کیمیائی خصوصیات کی تفہیم اور covalent bonds کی تعداد جاننے سے ہمیں کیمیاء کے اس دلچسپ شعبے میں مزید براہ راست معلومات حاصل ہوتی ہیں۔ C2H2 کی ساخت کو سمجھ کر ہم کیمیائی ری ایکشنز اور مادوں کے باہمی تعاملات کی گہرائی میں جا سکتے ہیں۔
Covalent bonds کی تعریف
جب ہم C2H2 مالیکیول کی بات کرتے ہیں، تو ہمیں سب سے پہلے *Covalent bonds کی تعریف سمجھنی ہوگی۔ Covalent bonds ایک قسم کے کیمیائی بانڈ ہیں جن میں دو ایٹمز اپنے الیکٹرانز کو بانٹتے ہیں۔ اس عمل میں، ایٹمز مل کر ایک مستحکم ساخت بناتے ہیں۔
یہ بانڈز اکثر غیر دھاتی عناصر کے درمیان بنتے ہیں، جہاں ایٹمز کی الیکٹرانز کی ضرورت کو پورا کیا جا سکتا ہے۔ C2H2، جو کہ ایسیٹائلین کے نام سے جانا جاتا ہے، میں یہ بانڈز خاص طور پر اہم ہیں۔
یہ بھی پڑھیں: Myofolic Sachet کے فوائد اور استعمالات اردو میں
Covalent bonds کی خصوصیات
Covalent bonds کی کچھ اہم خصوصیات یہ ہیں:
- مضبوطی: یہ بانڈز بہت مضبوط ہوتے ہیں اور عام طور پر ٹوٹنا مشکل ہوتا ہے۔
- ملاپ: دو ایٹمز کے درمیان یہ بانڈز مل کر ایک نئی مادے کی تشکیل کرتے ہیں۔
- پولرٹی: بعض Covalent bonds، جیسے کہ H2O میں، پولر ہوتے ہیں، جب کہ دوسرے غیر پولر ہو سکتے ہیں۔
- اپنی شکل کی موجودگی: Covalent bonds کے ساتھ مالیکیولز کی خاص شکل کے حامل ہوتے ہیں۔
یہ بھی پڑھیں: Roxvita Tablet کیا ہے اور اس کے استعمال اور سائیڈ ایفیکٹس
C2H2 میں Covalent Bonds
C2H2 مالیکیول کی ساخت میں، ہر کاربن (C) ایٹم ایک s-orbital اور p-orbital میں اپنے الیکٹرانز کو بانٹتا ہے، جس سے دو Covalent bonds بنتے ہیں۔ یہ bonds کاربن ایٹمز کے درمیان اور ہر کاربن اور ہائیڈروجن (H) ایٹم کے درمیان ہوتی ہیں۔
اس کے علاوہ، C2H2 میں ایک triple bond بھی موجود ہے، جو دونوں کاربن ایٹمز کو ایک دوسرے کے ساتھ جوڑتا ہے۔ یہ triple bond ایک sigma bond اور دو pi bonds کا مجموعہ ہوتا ہے، جو اسے ایک منفرد اور مستحکم ساخت فراہم کرتا ہے۔
یہی وجہ ہے کہ Covalent bonds کا مطالعہ کرنے سے ہمیں مالیکیولز کی کیمیا اور ان کے خواص کے بارے میں اہم معلومات حاصل ہوتی ہیں۔ C2H2 کے مثالی مطالعے کی مدد سے، ہم یہ سمجھ سکتے ہیں کہ کس طرح ایٹمز ایک دوسرے کے ساتھ مل کر مضبوط اور مختلف مالیکیولز بناتے ہیں۔
یہ بھی پڑھیں: پپیتا کے صحت کے فوائد اور استعمالات اردو میں
C2H2 میں bonds کی تعداد
C2H2 مالیکیول، جسے ایسیٹیلین بھی کہا جاتا ہے، ایک دلچسپ کیمیائی ترکیب ہے۔ اس مالیکیول میں بنیادی طور پر کاربن اور ہائیڈروجن ایٹمز موجود ہوتے ہیں۔ جب ہم اس کی ساخت کی بات کرتے ہیں، تو یہ سمجھنا ضروری ہے کہ C2H2 میں bonds کی کتنی تعداد ہے۔
C2H2 میں دو کاربن ایٹمز اور دو ہائیڈروجن ایٹمز ہوتے ہیں۔ اس مالیکیول کی اہم خصوصیات میں شامل ہیں:
- کاربن اٹمز: 2
- ہائیڈروجن اٹمز: 2
- C2H2 کی ساخت: سیدھی، خطی شکل
اب ہم C2H2 میں موجود covalent bonds کی تعداد کو دیکھتے ہیں:
C2H2 میں موجود bonds کی وضاحت
C2H2 میں بنیادی طور پر درج ذیل bonds موجود ہیں:
| Bonds کی قسم | کی تعداد |
|---|---|
| C–C bond | 1 |
| C≡C bond | 1 |
| C–H bond | 2 |
C–C bond یعنی کاربن کے درمیان ایک triple bond ہے، جس کی وجہ سے یہ مالیکیول مضبوط اور مستحکم ہے۔ اس کے علاوہ دو C–H bonds بھی ہیں، جو ہر کاربن ایٹم کو ایک ایک ہائیڈروجن ایٹم کے ساتھ جوڑتے ہیں۔
اس طرح، C2H2 میں کل تین covalent bonds ہیں: ایک triple bond جس میں دو کاربن ایٹمز ہیں اور دو single bonds جو ہائیڈروجن ایٹمز کو جوڑتے ہیں۔ یہ bonds اس مالیکیول کی خصوصیت کو واضح کرتے ہیں اور اس کی کیمیائی سرگرمی میں اہم کردار ادا کرتے ہیں۔
لہذا، اگر آپ C2H2 کی کیمیائی ساخت میں دلچسپی رکھتے ہیں یا اس کی خصوصیات سمجھنا چاہتے ہیں، تو اس کی bonds کی تعداد اور نوعیت کا جاننا بہت ضروری ہے۔
یہ بھی پڑھیں: How to Apply for Canada Work Visa in Urdu
C2H2 کے molecular characteristics
C2H2، جسے ایسیٹیلین کے نام سے بھی جانا جاتا ہے، ایک اہم دوہری مالیکیول ہے جو کیمیا میں خاص اہمیت رکھتا ہے۔ آئیے اس کے molecular characteristics پر نظر ڈالتے ہیں:
1. مالیکیولر فارمولا:
C2H2 کا مالیکیولر فارمولا یہ ظاہر کرتا ہے کہ یہ دو کاربن (C) ایٹمز اور دو ہائیڈروجن (H) ایٹمز پر مشتمل ہے۔
2. ساخت:
C2H2 کی ساخت تکمیلی دوہری بانڈ کے ساتھ ہے۔ یہاں کاربن ایٹمز آپس میں ایک دوہری covalent bond قائم کرتے ہیں، اور ہر کاربن ایٹم ایک ہائیڈروجن ایٹم کے ساتھ ایک سادہ covalent bond بناتا ہے۔
3. covalent bonds کی تعداد:
C2H2 میں ایک دوہری covalent bond ہے جو دو کاربن ایٹمز کے درمیان ہوتا ہے۔ اس کے علاوہ، ہر کاربن اور ہائیڈروجن کے درمیان ایک ساده covalent bond ہوتا ہے۔ لہذا، مجموعی طور پر C2H2 میں 3 covalent bonds موجود ہیں:
- 1 دوہری covalent bond (C=C)
- 2 سادہ covalent bonds (C-H)
4. سٹیریو کیمسٹری:
C2H2 کی ساخت میں لکیری* جئو میٹری موجود ہے، جس کا مطلب ہے کہ مالیکیول میں کاربن ایٹمز کے درمیان زاویہ 180 ڈگری ہے۔ یہ خصوصیت اس کی کیمیائی خصوصیات کو متاثر کرتی ہے، جیسے کہ اس کی ریاکشن کی نوعیت۔
5. خصوصیات:
C2H2 کی کچھ اہم خصوصیات یہ ہیں:
| خاصیت | تفصیل |
|---|---|
| گھلاؤ | C2H2 پانی میں اچھی طرح نہیں گھلتا۔ |
| جلنے کی خصوصیت | یہ ایک قابل احتراق گیس ہے اور ہلکے نیلے شعلے میں جلتا ہے۔ |
| درجہ حرارت | C2H2 کا نقطہ ابال 25.1 °C ہے۔ |
اس طرح، C2H2 کا molecular characteristics اس کی کیمیائی سرگرمیوں اور استعمالات میں فیصلہ کن کردار ادا کرتا ہے۔ یہ خاصیتیں اسے کیمیا اور صنعتی ایپلی کیشنز کے لئے ایک اہم مالیکیول بناتی ہیں۔
یہ بھی پڑھیں: پاکستان میں سب سے زیادہ پائی جانے والی 10 بیماریاں
Covalent bonding کی مثالیں
C2H2، جسے ایسرین یا ایٹیلین بھی کہا جاتا ہے، میں covalent bonds کی ایک دلچسپ مثال موجود ہے۔ یہ مالیکیول دو کاربن ایٹمز اور دو ہائیڈروجن ایٹمز پر مشتمل ہوتا ہے۔ چلیں، ہم covalent bonding کی مزید تفصیلات پر بات کرتے ہیں۔
یہ بھی پڑھیں: Mom C Tablet کیا ہے اور اس کے فوائد اور سائیڈ ایفیکٹس
کے لازمی نکات
- کاربن ایٹمز: C2H2 میں دو کاربن ایٹمز ہیں جو کہ ایک دوسرے کے ساتھ triple bond (تھریپل بانڈ) کے ذریعے جڑے ہوئے ہیں۔
- ہائیڈروجن ایٹمز: ہر کاربن ایٹم ایک ہائیڈروجن ایٹم کے ساتھ single bond کے ذریعے جڑتا ہے۔
اس طرح، C2H2 میں کل ملا کر 3 covalent bonds ہیں: 1 triple bond اور 2 single bonds۔ یہ bonds اس بات کی مثال ہیں کہ کس طرح ایٹمز آپس میں جڑے ہو سکتے ہیں تاکہ ایک مستحکم مالیکیول بنایا جا سکے۔
covalent bonds کی اقسام
| Bond Type | عددی حساب | شرح |
|---|---|---|
| Single Bond | 1 | دو ایٹمز کے درمیان ایک pair of electrons |
| Double Bond | 2 | دو ایٹمز کے درمیان دو pairs of electrons |
| Triple Bond | 3 | دو ایٹمز کے درمیان تین pairs of electrons |
Covalent bonding کی یہ مثالیں نہ صرف C2H2 کو سمجھنے میں مدد کرتی ہیں بلکہ عمومی طور پر moleculer structures کے بارے میں بھی ایک واضح تفہیم فراہم کرتی ہیں۔ مختلف ایٹمز کے درمیان bonding کی شدت اور نوعیت ان کی خواص پر براہ راست اثر ڈالتی ہے۔ اس سیاق و سباق میں، C2H2 کی مثال ایک ضروری درسگاہ فراہم کرتی ہے کہ کس طرح covalent bonds، ایٹمز کی فزیکل اور کیمیکل خصوصیات کو متاثر کرتے ہیں۔